Introduction
Le vieillissement des organismes a été appréhendé en laboratoire, tant sur les protozoaires (êtres unicellulaires) que sur les métazoaires (groupe d’organismes pluricellulaires, désignant les animaux), par des approches multiples, en relation avec la discipline des chercheurs. Ainsi trouverons-nous dans la littérature scientifique de nombreux articles, sur le thème de la sénescence, de spécialistes en génétique, en génomique, en biochimie des protéines, en métabolisme, en physiologie mais également de biologistes du développement embryonnaire (l’ontogenèse), d’écologues ou de chercheurs travaillant sur l’histoire évolutive des espèces (la phylogenèse). Mais aucune des données apportées par ces travaux de spécialistes, en soi d’importance, ne se suffit à elle-même pour répondre à cette question fondamentale, tant réclamée par Cavanna : pourquoi vieillit-on ? Car le vieillissement, partagé par tous les organismes vivants, est un phénomène biologique multifactoriel et complexe.
Nous présentons ici les avancées dans ce domaine de recherche selon deux temporalités : l’état des lieux, théories et observations en laboratoire, tels que nous pouvions le présenter à Cavanna, lors de notre rencontre avec lui au siège des journaux Hara-Kiri et Charlie-Hebdo, à Paris, en 19782. Puis sera présenté, dans une seconde partie, un éventail des connaissances scientifiques produites, depuis 1978 jusqu’à cette année 2025, sur la sénescence. Deux remarques :
1. Il ne sera question ici que du vieillissement des organismes car nous adressant fictivement aujourd’hui à Cavanna, comme nous avions pu le faire réellement en 1978, nous avons volontairement évité de parler du vieillissement des populations, sujet qui n’apparaît jamais dans son Stop-Crève, sa préoccupation essentielle étant de ne point vieillir en tant qu’individu.
2. Le transhumanisme, en tant que mouvement idéologique scientiste prétendant à la disparition prochaine des pathologies ainsi que du vieillissement, ne peut être omis et sera analysé dans sa dimension épistémologique. C’est une vision du monde robotisé, hyper technocratique, dominé par l’« intelligence » artificielle qui n’aurait, pensons-nous, guère plu à Cavanna, lui qui aimait tant la vie… tout simplement, mais si complètement, la vie.
Sur la sénescence des organismes. Hypothèses et faits expérimentaux en 1978
En laboratoire, l’explication du vieillissement des organismes se pensait soit dans le cadre de l’hypothèse de la programmation génétique soit dans celui des erreurs et des dommages. Dans le premier cas, la sénescence serait la dernière étape d’un calendrier biologique qui commencerait par le développement de l’individu. Une sorte d’horloge interne, après un certain temps d’existence ou de fonctionnement de l’organisme, donnerait le signal de départ d’un processus physiologique conduisant au vieillissement puis à la mort de l’individu. Le rôle d’un contrôle génétique, dans cette hypothèse, était supposé mais cela restait vague. Certes, chaque espèce a globalement une longévité qui lui est propre : ainsi, l’espérance de vie d’une souris est bien courte en regard de celle de l’humain. Mais cela n’explique pas, dans l’espèce humaine, l’allongement de la durée de la vie depuis plusieurs siècles (quelques quarante années supplémentaires en deux siècles dans les pays industrialisés) ni sa disparité, toute relative, entre les individus d’une même espèce dans les mêmes conditions environnementales. Si une corrélation trop facilement admise veut que plus un organisme est volumineux plus son espérance de vie est longue (la souris contre l’homme ou l’éléphant), que penser de la chauve-souris qui vit 10 à 20 fois plus longtemps que son équivalent murin en taille, du cheval contre l’âne ou le chameau avec leurs 25, 40 ou 50 années respectives de longévité ? Dans l’état des connaissances en 1978, expliquer le vieillissement par une programmation inscrite dans le génome était une hypothèse décrite parfois dans la littérature. Dans cette idée, dans les années 1950, Georges Williams, reprenant la théorie de Peter Medawar sur la sénescence occasionnée par des mutations dans l’ADN3, propose une théorie singulière. Des gènes ayant des effets bénéfiques pour l’organisme, surtout avant la reproduction, deviennent après celle-ci néfastes. Ils deviennent alors des « gérontogènes », induisant le vieillissement. Il nomme ce phénomène « pléiotropie antagoniste ».
Dans la seconde hypothèse, celle des erreurs, les tissus présenteraient des dysfonctionnements métaboliques à cause d’erreurs, de plus en plus mal réparées, produites dans les innombrables réactions biochimiques cellulaires. Ces erreurs peuvent être occasionnées par exemple par une malformation de la structure tridimensionnelle d’enzymes, ou de leurs sites catalytiques (sièges de toutes réactions chimiques dans le vivant) dont les conséquences peuvent être très préjudiciables sur l’homéostasie cellulaire ou les fonctions des cellules dans un tissu donné. Une des causes majeures de ces malformations dans l’architecture (et donc le fonctionnement) des composants moléculaires des cellules (d’êtres uni- ou multicellulaires) provient de mutations stochastiques dans l’ADN génomique. Certaines mutations dans l’ADN peuvent avoir des effets délétères, tant sur la réplication du génome lors des mitoses (divisions) cellulaires, ou sur les transcriptions de l’ADN en ARN messagers, lors de l’expression génomique, puis dans la lecture par les ribosomes de l’ARN messager en protéines. Les molécules ainsi mal synthétisées pour de multiples raisons dans la chaîne de synthèse perturbent alors le métabolisme cellulaire et peuvent engendrer la mort cellulaire. Comme l’ADN génomique, l’ADN mitochondrial est l’objet de mutations. Celles-ci altèrent de multiples façons les fonctions des mitochondries, classiquement décrites comme les centrales énergétiques de la cellule. Rappelons que les mitochondries ne sont transmises que par la mère. Les radicaux libres, issus du métabolisme normal de la cellule, peuvent être aussi source d’altération. Ces derniers sont des atomes ou des molécules ayant perdu un électron, devenus dès lors très réactifs, qui induisent un processus d’oxydation au niveau de nombreuses structures fondamentales de la cellule, les mitochondries en particulier. On parlera alors de stress oxydant. Notons toutefois que ces radicaux libres (appelés ERO, pour Espèces Réactives de l’Oxygène) ne sont pas forcément toxiques. Ils sont décrits actuellement (ce n’était pas le cas en 1978), dans les conditions normales de leurs productions, comme un mécanisme essentiel de la signalisation cellulaire participant à l’homéostasie de la cellule.
Les conséquences en cascade de ces « erreurs catastrophes » affectent le fonctionnement physiologique de l’organisme et seraient une des causes du vieillissement de celui-ci. Il est possible qu’avec l’âge, ces erreurs surviennent plus fréquemment. Notons aussi que l’âge suscite un épuisement des glandes secrétant les hormones anabolisantes (hormone de croissance) alors que, en même temps, les taux d’hormones catabolisantes (qui diminuent le volume tissulaire) sont en augmentation.
Dans la seconde hypothèse toujours, les perturbations dans le fonctionnement complexe du métabolisme cellulaire et de la physiologie de l’organisme peuvent provenir non de causes internes comme décrites précédemment mais de causes externes. Par les dommages subis lors d’agressions de toutes sortes (agents chimiques toxiques, radicaux libres, rayonnements ionisants, radiations UV, stress…) le corps subit constamment les atteintes du temps. Cependant, l’organisme répare en permanence les erreurs et les dommages. Un exemple : les facteurs environnementaux ou erreurs internes dans le métabolisme cellulaire produisent plusieurs milliers de lésions de l’ADN par cellule et par jour, affectant l'intégrité du chromosome. Différentes sondes vont reconnaître les structures anormales présentes au sein de l'ADN (bases nucléiques modifiées, pontages ADN-protéines, cassures simples ou double brin, etc.) et les réparations vont immédiatement opérer, par des mécanismes sophistiqués mais précis impliquant des enzymes spécifiques (endo- et exo-nucléases, glycosylases, polymérases, ligases…). Mais avec l’âge, vitesse et taux de réparations vont diminuer.
Durant le développement de l’embryon et plus tard dans l’organisme adulte, les cellules participant aux différentes organogenèses ou au renouvellement tissulaire permanent vont se multiplier4. Mais cette capacité à la division a toutefois une limite. Ainsi, des cellules en culture, tels les fibroblastes, ne se divisent pas plus de 50 fois environ, phénomène décrit comme la limite de Hayflick5. Passé ce nombre de divisions, les cellules entrent en sénescence dite réplicative, puis meurent. Ainsi les cellules de notre corps ont un taux fini de renouvellement. Les cellules composant les organes d’un organisme très âgé atteindraient alors cette limite de Hayflick. Ceci se confirme dans des cultures de fibroblastes de donneurs jeunes ou âgés. In vitro, les fibroblastes de donneurs jeunes se divisent de nombreuses fois alors que ceux de donneurs âgés très peu. Nous reviendrons plus loin sur cette donnée importante. Notons que les cellules qui échappent à cette règle, qui se divisent sans limite, sont les cellules souches embryonnaires, indifférenciées donc totalement immatures, ou bien les cellules dites transformées, c’est-à-dire cancéreuses, malignes.
La documentation scientifique apportée à Cavanna, lors de notre rencontre en 1978 au siège de Charlie, Charlie-Hebdo et Hara-Kiri (cf. figure 1), portait sur ces données que nous venons de présenter.
Figure 1. Cavanna en 1978 au siège des journaux Charlie Hebdo, Hara-Kiri et Charlie mensuel, rue des Trois-Portes, Paris Vème.
L’état des connaissances en biologie de la sénescence ne permettait nullement à cette époque d’entrevoir la possibilité en laboratoire de ralentir le vieillissement ou de provoquer un état physiologique qui pourrait évoquer un rajeunissement. La teneur de notre entrevue avec Cavanna, purement scientifique, donc rationaliste matérialiste (Cavanna n’attendait d’ailleurs de notre part rien d’autre que cela), a certainement été décevante pour lui. « Stop-Crève » c’est-à-dire une jeunesse prolongée, à tout le moins une inhibition du vieillissement, a dû lui paraître hors de portée.
Mais en 2025, est-ce toujours le cas ? Pratiquement un demi-siècle après cette rencontre, si cette entrevue avait pu se reproduire aujourd’hui (Cavanna est décédé en 2014), quels progrès majeurs dans la compréhension de la sénescence du vivant pourraient lui être présentés ? Ainsi, des faits expérimentaux stupéfiants pour les biologistes en 1978, ayant une nature de révolution paradigmatique6, ont-ils été décrits dans la littérature en ce début du XXIe siècle. Résultats en laboratoire qui auraient pu enthousiasmer l’auteur de Stop-Crève et le conforter dans son assertion : « le vieillissement n’est pas une évolution "normale", "naturelle" (j’insiste sur les guillemets) de la matière vivante7 ». Mais ces mêmes progrès scientifiques ne font-ils pas surgir aussi des réserves sur une possible « thérapie anti-âge » vantée un peu trop rapidement par certains, réserves nourries par la compréhension même de l’immense complexité, dans un être vivant, des interactions moléculaires et cellulaires ? Ces formidables avancées en biologie de la sénescence, obtenues dans ce début de XXIe siècle, passionnantes pour le biologiste, autorisent-elles vraiment de prochains traitements efficaces contre le vieillissement du corps humain, dans son soma comme dans sa psyché ?
Sur la sénescence des organismes. Hypothèses et faits expérimentaux de 1978 à 2025
Beaucoup d’avancées en biologie cellulaire et dans le développement des organismes sont décrites dans la littérature internationale (les revues scientifiques académiques) révélant des phénomènes insoupçonnés en 1978. Le prix Nobel 2012 Shinya Yamanaka a réussi, dans une astucieuse manipulation in vitro, à faire revenir des cellules différenciées (de muscle, de foie, d’épiderme, etc.) à l’état de cellules embryonnaires, indifférenciées. Ce sont les cellules souches pluripotentes induites (IPSC en anglais), capables ensuite d’être réorientées, selon les conditions de culture, vers une nouvelle différenciation et pas forcément celle d’origine8. Suite à ces travaux du laboratoire japonais, décrits d’abord sur le modèle murin (la souris) puis sur des cellules humaines en 2007, de nombreux chercheurs se sont lancés dans l’étude de ce phénomène passionnant. En 2011, une équipe de l’Institut de Génomique Fonctionnelle de Montpellier a fait « exploser » la limite de Hayflick9 ! Ainsi, des cellules de peau de centenaires, incapables de se multiplier in vitro car sénescentes, redevenues cellules souches IPSC puis réorientées en cellules épidermiques, ont pu se rediviser, comme si elles avaient été prélevées sur un jeune homme.
Arrêtons-nous sur ces données. Dans les années 1970-80, il était considéré comme admis et indépassable que :
- Toute cellule immature (une cellule souche embryonnaire) devenue différenciée (en neurone, hépatocyte, fibroblaste, leucocyte, ostéoblaste, macrophage, etc.) ne peut revenir en arrière et redevenir une cellule souche10.
- Toute cellule différenciée normale (au sens de non transformée, non cancéreuse) ayant effectué un nombre de divisions proche de sa limite de Hayflick, ne peut qu’entrer en sénescence puis mourir. Tout « rajeunissement » est impossible.
Nous observons que ces assertions qui allaient de soi en biologie cellulaire, tant dans les laboratoires de recherche que dans l’enseignement à l’université, il y a quelque cinquante ans, découlaient d’observations expérimentales constamment renouvelées en laboratoire, que rien, dans l’état des connaissances et des technologies à cette époque, ne permettait de reconsidérer. L’on voit que ce paradigme scientifique est maintenant totalement remis en cause, en laboratoire, par les travaux sur les IPSC ! En science, les connaissances progressent parfois, non de façon graduelle, mais par des sauts qualitatifs majeurs permis par des éclairages nouveaux venant de « découvertes » inattendues. Des théories novatrices bousculent alors les paradigmes établis, c’est une révolution scientifique comme l’a soutenu le philosophe des sciences Thomas Kuhn11.
Revenons sur cette limite de Hayflick dans les conditions normales de cellules différenciées se divisant. Pourquoi les cellules vieillissantes perdent-elles leur capacité à se multiplier ? Une piste est celle des télomères. Découverte dans les années 80, cette étrange structure d’ADN non codant, couvrant l’extrémité des chromosomes, raccourcit à chaque réplication chromosomique, prélude à la division de la cellule (mitose). Chez l’humain un télomère de quelques 10 Kbp12 se voit diminuer de 100 à 200 bp à chaque division cellulaire. Sa disparition laisse les chromosomes ouverts, la cellule ne se divise plus, aboutissant à sa mort par apoptose (terme qui désigne la mort programmée, active, et non par nécrose, passive, d’une cellule). En 2010, il a été montré que par la réactivation d’une enzyme, la télomèrase inverse transcriptase, les télomères peuvent cesser de se raccourcir, voire s’allonger. Attention, cette propriété d’avoir de longs télomères (signe de jeunesse ?) est celle des cellules souches et aussi… celle des cellules malignes, cancéreuses.
L’on parle ici de cellules. Mais de même que le fonctionnement cellulaire n’est pas réductible aux seuls gènes, pensons par exemple à l’épigénétique (les facteurs environnementaux qui peuvent allumer ou éteindre l’expression d’un gène13), de même l’étude du vieillissement d’un organisme n’est pas réductible à celui de ses cellules isolées. Alors qu’en est-il par exemple pour un organisme pluricellulaire, un métazoaire ? Prenons le nématode Caenorhabditis elegans, un des plus simples d’entre eux, un ver de 1 mm de long, possédant 959 cellules, 302 neurones et 19099 gènes. Arrêtons-nous sur cela, comparons ce petit ver avec nous. L’humain a un peu plus de 30 000 milliards de cellules, entre 80 et 100 milliards de neurones mais… une quantité de gènes, un peu plus de 20 000, du même ordre de grandeur que celle du ver. Cavanna aurait aimé ce genre de comparaison qui, aurait-il dit, « donne à penser » ! Notons que les biologistes, autour des années 1980-90, dans cette représentation d’alors que le biologique est réductible au tout génétique, estimaient le nombre de gènes chez Homo sapiens autour de 100 000 et, quelques décennies auparavant, à plusieurs millions. Deux remarques s’imposent ici : premièrement, dans sa fantasmée « supériorité » sur les autres espèces, l’homme « se devait », à cette époque, d’avoir un tel nombre de gènes. Beau présupposé ! Deuxièmement, avec 20 000 gènes, comme le ver ou la mouche, nous sommes pour autant bien différents. Soulignons ainsi, dans l’ensemble du vivant, l’importance et la complexité des événements moléculaires qui opèrent avant, pendant et après l’expression des gènes, modulant finement ces expressions. C’est cette complexité adaptative du génome et de l’épigénome14 qui permet aussi la spéciation, c’est-à-dire l’apparition de nouvelles espèces et, partant, de leurs évolutions. Ce petit ver est un des animaux fétiches des laboratoires pour l’étude des bases cellulaires, génétiques et moléculaires du développement (avec la souris Mus musculus, la mouche Drosophila melanogaster et le poisson zèbre Danio rerio). Il l’est également pour l’étude du vieillissement15. Ainsi, la littérature scientifique rapporte en ce domaine, dans le cas du Caenorhabditis elegans, plusieurs facteurs moléculaires induisant un phénotype pro-longévité ou pro-vieillissement. Certains sont les produits de gènes orthologues (présentant des similarités évolutives) à 80 % à leurs équivalents humains. La simplicité anatomique du ver est un atout mais aussi une faiblesse. C’est un invertébré donc il n’a pas de squelette. Mais également il n’a pas de cerveau, de cœur, de reins ni de système vasculaire pour les irriguer. Les limites sont évidentes pour une transposition à l’humain. Qu’en est-il alors pour des organismes beaucoup plus complexes, tels ceux de vertébrés comme le poisson zèbre ou, plus encore, de mammifères comme le tamia rayé (Tamias striatus) ou la souris ? En 2023, des chercheurs de l’INSERM ont montré, chez Danio rerio, que l’activation de la télomérase16 dans l’intestin de ce poisson et, conséquemment, l’allongement des télomères dans les cellules épithéliales intestinales, avait un effet antivieillissement sur cet organe et, de façon surprenante, sur tout l’organisme17. Ce qui va dans le sens, généralement admis, que le vieillissement est corrélé avec une diminution de la taille des télomères. Mais, comme pour bien rappeler que toute assertion ayant vite un caractère de généralité doit être prise avec précaution en science et tout particulièrement en science du vivant, une équipe canadienne a montré, peu de temps auparavant que, chez le petit écureuil Tamias striatus, ces télomères ne raccourcissent pas avec l’âge et peuvent même, en fonction de leur « train de vie » lié à leur reproduction, s’allonger18. Chez la souris, en s’inspirant des travaux du prix Nobel 2012 Shinia Yamanaka sur les cellules souches pluripotentes induites (IPSC), puis des données de l’équipe française en 201119 sur le retour à des propriétés juvéniles de cellules différenciées de donneurs très âgés, via leur passage à l’état immature d’IPSC, plusieurs laboratoires ont utilisé dernièrement le principe de cette méthodologie, non plus sur des cellules isolées in vitro, mais sur des organismes entiers adultes in situ. Rappelons ici que cette méthodologie dite OSKM repose sur l’expression ectopique (qui ne se trouve pas à sa place habituelle) de quatre facteurs de transcription20 Oct4, Sox2, Klf4, c-Myc (OSKM). Ces molécules, appelées depuis « facteurs de Yamanaka », ont la propriété d’agir rétro-temporellement sur l’épigénèse de l’ADN (portant sur les modifications structurelles dans le temps des bases moléculaires de l’ADN et non sur leurs séquences). Une hypothèse est que cette action permettrait de restaurer la jeunesse des cellules.
Ces études ont rapporté des effets « rajeunissants » présents dans quelques tissus (mais pas tous), tels qu’une réversion de l’horloge épigénétique (modifications moléculaires du génome, tels des méthylations de l’ADN), ou des modifications du métabolisme et du transcriptome (état fonctionnel du génome21). Selon certains auteurs, un tel traitement observé sur la souris correspondrait, avec toutes les précautions qui s’imposent dans ce type de comparaisons, à faire rajeunir un humain de plus de soixante ans d’une dizaine d’années22. Cependant, il est rapporté aussi que ce traitement occasionne un vieillissement sur des tissus voisins de ceux « rajeunis ». D’autre part le sexe de l’animal ou son âge peuvent moduler les résultats. Ainsi la peau de souris femelle est-elle plus sensible au traitement rajeunissant OSKM que la peau de souris mâle. De plus, un animal très âgé devient insensible à cet effet OSKM. Plusieurs hypothèses sont proposées dans la littérature. Mais ici encore la prudence s’impose : dans ces cas d’augmentation de la longévité, qu’en est-il des capacités cognitives, immunitaires ou reproductives, par exemple, de ces organismes dits « rajeunis » ? On pourra imaginer Cavanna s’interrogeant sur ces questions d’importance…
Des travaux très récents, encore débattus, montreraient l’existence d’une nouvelle forme de communications cellulaires : les nanotubes. Ces structures fines permettraient un transfert d’informations entre cellules, présentes lors du développement embryonnaire23, ou entre éléments cellulaires dans le cerveau24. L’on peut formuler l’hypothèse que ces nanotubes puissent être impliqués dans les processus de la sénescence.
Depuis une décennie, la littérature scientifique décrit de multiples approches originales, expérimentées en laboratoire dans des modèles animaux. La restriction calorique25 ayant été décrite comme pouvant allonger l’espérance de vie de divers organismes, plusieurs molécules mimant cette restriction sont testées sur l’animal, mais également sur l’humain dans le cadre de larges essais portant sur plusieurs milliers de personnes. C’est l’étude américaine TAME (Targeting Aging with Metformin) suivie actuellement par quatorze instituts de recherche. Une autre piste consiste à tester des protocoles pouvant contrer les effets des molécules délétères sécrétées par les cellules vieillissantes. Ces molécules ne sont pas nocives en soi mais elles le deviennent quand elles sont produites de façon inappropriée : cytokines pouvant déclencher des réactions inflammatoires, protéases détruisant la matrice extracellulaire, facteurs de croissance en excès ou insuffisants… Au cours de la sénescence, de profonds remodelages morphologiques et fonctionnels affectent les tissus âgés. Ces phénomènes génèrent un phénotype26 sécrétoire spécifique appelé sécrétome associé à la sénescence ou SMS (senescence-messaging secretome). Ce SMS est activement étudié car il modifie l’homéostasie27 et le microenvironnement tissulaires. C’est ainsi un indicateur de sénescence. De très nombreuses « sénothérapies » innovantes dans l’espoir de contrer le vieillissement de l’organisme et des pathologies qui y sont associées sont rapportées dans la littérature28. Deux principales voies sont envisagées concernant les sénothérapies anti-SMS. La première s’intéresse aux inhibiteurs de la production des molécules nocives dites « sénomorphes » produites par les cellules vieillissantes. La deuxième approche porte sur des processus dits « sénolytiques » visant à la destruction de cellules sénescentes, par l’emploi de molécules provoquant in fine la clairance des cellules âgées, donc leur disparition. Cette élimination des cellules vieillissantes pourrait être envisagée par le système immunitaire, que l’on cherchera à stimuler spécifiquement. Toutefois, deux remarques importantes ici : premièrement, ce système immunitaire vieillit lui aussi et son efficacité diminue et, deuxièmement, les cellules sénescentes peuvent être une barrière, dans certains cas, à la progression tumorale par exemple et donc avoir une réelle importance dans certaines conditions physiologiques. Supprimer des cellules âgées (et lesquelles ?) pourrait avoir de graves conséquences inenvisageables actuellement. Dès lors, un protocole simpliste portant sur un événement métabolique, fût-il prometteur en laboratoire dans le cadre d’un traitement sénolytique, peut s’avérer délétère, par un effet cascade d’effets secondaires fâcheux. L’on comprendra la nécessité d’avoir la meilleure compréhension globale possible de l’extrême diversité des interactions physiologiques opérant dans des organismes jeunes ou âgés.
Nous ne pourrions dire autre chose à Cavanna dans une entrevue fictive aujourd’hui, malgré les impressionnantes avancées, tant méthodologiques que conceptuelles, en biologie de la sénescence depuis 1978. De plus, lors de notre rencontre avec Cavanna à cette époque, nous ne pouvions discuter non plus de la mort cellulaire comme processus actif, nécessaire et indispensable à la physiologie d’un être vivant car cette notion n’était pas présente dans l’esprit des chercheurs et encore moins un sujet d’étude. L’idée que des cellules puissent se « suicider » au profit de l’organisme n’était pas encore, en 1978, dans la réflexion des biologistes. Nous allons développer ici, bien que brièvement, cette notion, fondamentale aujourd’hui en biologie, que la mort est indissociable au processus même de la vie. Nous nous plaisons à imaginer Cavanna méditant ce sujet : la mort comme instance indispensable à la vie. Que nous aurait-il écrit, de son style si direct et imagé, là-dessus ?
La mort, consubstantielle à la vie
En 1864, Bichat énonçait que la vie est « l’ensemble des fonctions qui résistent à la mort »29. C’est bien ainsi que l’exprimait Cavanna : « la matière vivante est une protestation contre la mort, contre le vieillissement30 ».
Mais, désolé cher Cavanna, on ne peut plus définir ainsi le vivant aujourd’hui ! La mort (cellulaire) est partie prenante intrinsèquement du processus vivant. Claude Bernard, en son temps, avait eu cette formidable intuition en disant : « la vie c’est la mort » et, ajoutant aussitôt : « la vie c’est la création31 ». Au cours du développement de l’embryon (humain, pour prendre un exemple qui aurait fortement intéressé Cavanna) des « suicides » cellulaires sont observés. Cette autodestruction des cellules, encore appelée apoptose, ou mort cellulaire programmée, est un processus actif, contrairement à celui de la nécrose, purement passif. La mort cellulaire est un phénomène constitutif de l’embryogenèse. Citons, pour exemples, la disparition des palmes digitaux dans la morphogenèse de la main, l'involution différentielle des canaux de Wolff et de Müller au cours de la formation des voies génitales, la mort de neurones, très tôt, dans la morphogenèse cérébrale… Les mécanismes biologiques impliqués dans l’apoptose font l’objet d’un vaste champ de recherche. Cette idée de « suicide » cellulaire est relativement nouvelle en biologie et restée longtemps contre-intuitive : ainsi, un embryon se construirait autant par prolifération que par destruction cellulaire, le cancer pourrait survenir par arrêt des processus de mort cellulaire. Car cette mort programmée de cellules est présente aussi dans l’organisme mature, tout au long de la vie de l’individu. Elle est nécessaire à l’homéostasie tissulaire comme aux fonctions physiologiques, telle la sélection lymphocytaire dans la réaction immunitaire. Le corps se renouvelle en permanence : nous gagnons et perdons chaque année notre poids en cellules ! C’est, chez l’adulte, une permanente « embryogenèse silencieuse », pour reprendre ce joli terme du grand physiologiste Claude Bernard. Ce renouvellement constant des cellules doit de plus conserver l’architecture du plan de base du corps32 (non seulement au cours de l’embryogénèse mais après la naissance au cours de l’existence de l’individu), les fonctions physiologistes, et notre moi identitaire, qui font que « je » n’est pas un autre33. Ce moi est cependant évolutif, par les apprentissages tout au long de la vie, que les biologistes appréhendent tant au niveau génomique (structure de la chromatine) qu’au niveau anatomique dans le cerveau (architectures synaptiques). Le neurobiologiste du développement Alain Prochiantz nomme cette évolution biologique du moi individuation34. Ainsi, vie et mort, dans les organismes biologiques, sont dans un rapport dialogique, au sens décrit par Edgard Morin35 : sont dans un rapport dialogique deux instances complémentaires, antagonistes mais indissociables d’une même unité. Ainsi, prenons comme autre exemple la nature corpusculaire et ondulatoire de la lumière. Cette vision du vivant l’ancre dans le monde de la complexité.
Le développement des organismes et l’évolution des espèces : le vivant, monde de la complexité
Selon un point de vue évolutionniste, le vieillissement des individus n’opèrerait véritablement qu’une fois la reproduction de l’espèce assurée. Dans les cas extrêmes (sémelparité), la mort survient après l’accouplement. Pour les espèces itéropares, les individus peuvent se reproduire plusieurs fois. Grâce aux outils actuels de séquençages ultrarapides de l’ADN, des méta-analyses ont pu montrer que les espèces qui ont une durée de vie plus longue accumulent plus lentement des mutations génétiques. Soumises à des pressions de sélection variées, les espèces développent des stratégies d’adaptation ad hoc, qui sont en relation avec des modifications complexes au sein des organismes des individus. Selon la théorie darwinienne, l’évolution opère grâce à la variabilité au sein des espèces, assurant la descendance avec modifications des plus adaptés à des transformations majeures de l’environnement. Cette sélection opère sur un temps long. Si les individus deviennent immortels, cette variabilité des espèces pourra-t-elle opérer ? Si la mort est consubstantielle à la vie dans le développement puis l’existence d’un être vivant et si l’on veut transposer cela à l’échelle des espèces, la mort des individus serait alors nécessaire à l’évolution de celles-ci.
De données récentes dans les sciences du vivant a émergé l’idée d’un continuum entre l’évolution des espèces et la biologie du développement des organismes, un vaste champ de recherche appelé Evo-Devo36 ou ontophylogenèse37. Dans ce continuum, où opèrent le hasard et la nécessité38, la contingence et la contrainte39, le monde vivant révèle son essence fondamentale. Nous sommes alors dans le champ de la complexité. Alors opèrent les interactions constantes entre niveaux d’intégrons, au sens décrit par le prix Nobel François Jacob où les êtres vivants se construisent par l’empaquetage de niveaux (ou intégrons) discontinus, chacun formé par l’assemblage d’intégrons de niveaux inférieurs et participant à l’intégron de niveau supérieur40 (ex : …- la chimie des molécules biologiques - le fonctionnement cellulaire - le fonctionnement des organes - l’individu - société/culture/environnement…). Champ de la complexité aussi car le vivant est dans le monde des systèmes dissipatifs41 ou autopoïétiques42 et celui des auto-(géno-phéno) organisations43 : boucles de rétro-actions entre les niveaux d’intégrons constitutifs de l’être vivant et le monde extérieur (la société, la culture, l’environnement…).
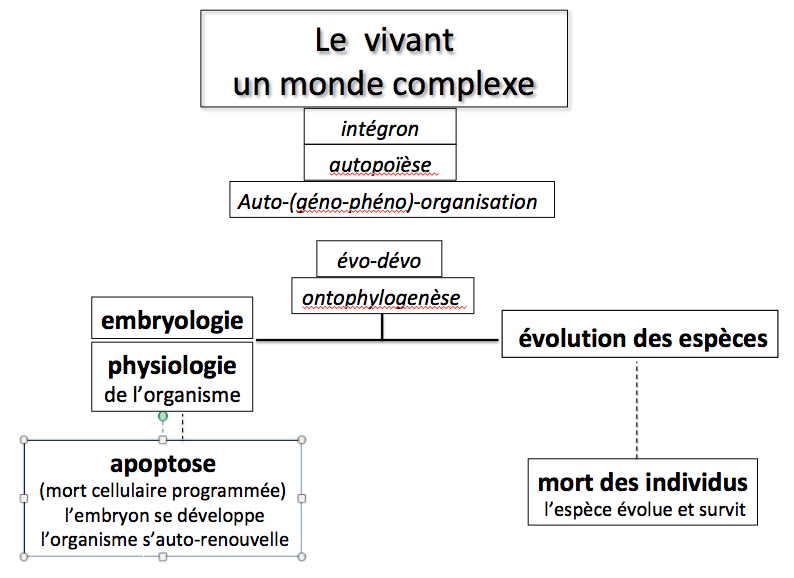
Le schéma rapporté dans la figure 2 résume le fait que le champ de la complexité est prégnant dans l’édification d’un être vivant (embryogénèse) comme dans son fonctionnement physiologique comme individu et dans l’espèce auquel il appartient, lequel est soumis à la pression évolutive. Et dans ce champ intervient aussi la mort cellulaire, celle des individus et celle des espèces.
Figure 2. Le vivant, champ de la complexité.
Sur le transhumanisme et autres idéologies néo-scientistes
Les prétentions à l’immortalité des transhumanistes, l’Homme « augmenté » (H+), portées par une foi en un supposé progrès techno-scientiste salvateur, révèlent une représentation du biologique absolument navrante et surtout une profonde inculture scientifique. Des explications purement mécanicistes44, ne portant, pour le problème du vieillissement du corps, que sur des thérapies simplistes, en privilégiant la partie (l’induction d’effecteurs moléculaires) et oubliant le tout (la physiologie de l’organisme dans sa dimension soma-cognition-émotions), nous semblent potentiellement dangereuses. La recherche fondamentale en sciences du vivant, dans les laboratoires académiques, est épistémologiquement, ontologiquement, différente car elle repose, en principe, sur la volonté d’appréhender les phénomènes dans leurs complexités, par un exercice collectif, entre pairs, d’interrogations permanentes des données d’expériences et des théories en cours, toute connaissance n’étant jamais définitive par essence. Le transhumanisme est une forme dévoyée de la technoscience privilégiant le spectaculaire au détriment des idées et de la réflexion dans un esprit mercantile et sans esprit critique. Une activité lucrative qui relève plus d’une sorte de religiosité technophile. Dans l’état actuel des connaissances donc, il nous semble difficile, en transposant trop rapidement ce qui est relevant de la cellule ou d’un tissu à un organisme entier, en oubliant la physiologie générale, de proposer une thérapie antivieillissement voire rajeunissante avec l’assurance de ne pas avoir de possibles effets secondaires… fort désagréables. La question demeure : ne pas vieillir est-il de l’ordre de l’utopie ou de la dystopie ? Immortalité, à quel prix ?
Interpellation imaginaire avec l’auteur de Stop-Crève
Si je pouvais discuter à nouveau avec toi, Cavanna, sur les avancées scientifiques dans la recherche sur le vieillissement, moi qui partageais totalement, en 1978 (et peut-être encore aujourd’hui ?), ton utopie de « Stop-Crève », que te dirais-je maintenant, en 2025 ? Mon enthousiasme pour les sciences du vivant demeure intact et je suis passionné par les avancées remarquables dans la biologie de la sénescence. Mais je ne pourrais faire autrement que formuler une grande prudence, pour les raisons exprimées plus haut, face aux battages médiatiques et à la frénésie de certains acteurs dans la sphère des GAFA et parfois, dans celle de la recherche académique. En restant uniquement dans le questionnement scientifique et sans aborder ici d’autres réflexions que l’on ne peut évacuer, d’ordres philosophiques, géopolitiques, éthiques, le prolongement de la vie en bonne santé pour l’humain, d’un état durable, sur un temps long, de jeunesse du corps et des fonctions cognitives par des « thérapies anti-âge », dans l’état actuel des connaissances en laboratoire, me semble bien périlleux. Ta ferveur pour la recherche scientifique, Cavanna, et tout particulièrement pour les sciences du vivant, mais tout autant ton esprit critique, ta rationalité sans cesse opérante, auraient très certainement perçu la complexité scientifique de ce problème.
De ton utopie, je retiens de toi Cavanna ta parole d’homme libre affirmant que la seule certitude que nous ayons est que nous n’avons qu’une vie. Tu écris :
C’est bon d’avoir faim, d’avoir soif, de manger, de boire, d’aimer, d’être aimé, de ne plus l’être, d’avoir peur, de se rassurer, d’ouvrir mes longues jambes maigres et de sentir le trottoir courir dessous, de regarder les pensées cavaler dans ma tête, de me dire que ça c’est le monde, et que ça, c’est moi, et que je suis dedans, et qu’on va drôlement bien ensemble, merde.
Les avancées dans la compréhension du phénomène de vieillissement de l’organisme, développées dans cet article, t’auraient sans nul doute donné matière à réflexion, toi qui aimais tant faire fonctionner… tes « boyaux de la tête ». Elles ne t’auraient cependant pas empêché de continuer à crier avec force, sur la volonté de vivre, encore et encore : « Alors, puisque ça a commencé, je ne veux pas que ça finisse. Fallait pas m’y faire goûter ! ».